

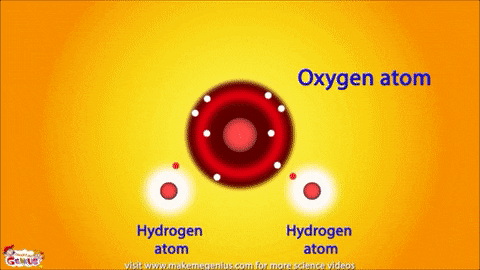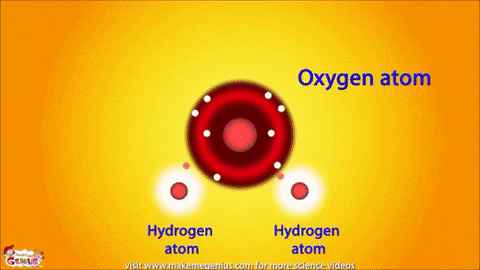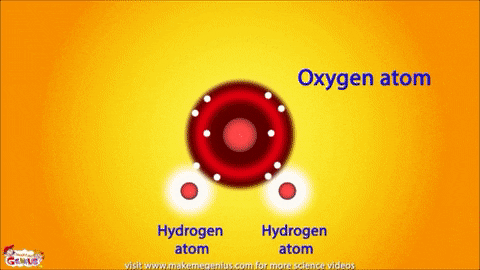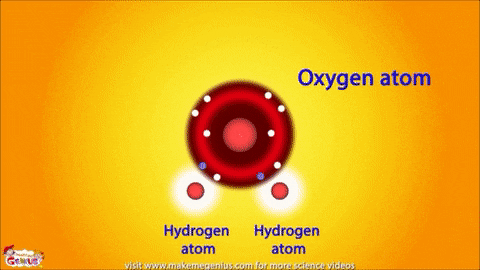

공유결합(共有結合, covalent bond)은 주로 비금속 원소들간의 결합이며, 안정된 전자 배열(s^2p^6)을 위해 원자들이 전자를 공유, 즉 함께 소유하고 있습니다. 공유 결합으로 이루어진 분자는 원자핵과 전자쌍 사이의 인력, 즉, 양전하를 띤 원자핵과 원자들의 공유 전자들 사이의 강한 쿨롱 인력, 그리고 원자간의 반발력에 의해 안정화되고 있죠. 공유 결합이 이루어지면 원자들은 일반 궤도와 모양이 다른 하이브리드 궤도에서 전자들을 공유하게 됩니다. 이온 결합의 경우 전기 음성도, 즉 전자를 받아들이는 정도의 차이와 전자에 대한 인력의 차이로 전하들이 분리되나 공유 결합에서는 전하가 분리되지 않거나(무극성 공유 결합), 분리가 되더라도 적은 정도로만 분리되어 있어(극성 공유 결합) 전자의 쏠림 현상이 크지 않습니다. 여기에서 무극성 공유 결합이란, 공유 결합을 이루는 원자들의 전기 음성도가 같은 경우이며, 전하의 분포가 균일하게 되어 분자는 무극성의 띄게 되죠. 반면에 극성 공유 결합에서는 원자들의 전기 음성도가 서로 달라서 전자들이 특정 방향으로 치우치면서 분자는 쌍극성, 즉 전하의 분리가 일어나게 됩니다. 물 분자가 대표적인데 산소의 전기 음성도가 수소보다 크므로 산소 쪽이 음(-), 수소 쪽이 양(+)의 전하를 띄는 전기 쌍극자를 이루게 됩니다.


공유 결합을 하는 물질은 이온 결합의 경우처럼 전자가 한 원자에서 다른 원자로 이동하는 것이 아닙니다. 전자가 한 원자에 속한 상태에서 다른 원자의 원자핵에도 끌리는 경우이죠. 즉, 전자들은 두 개 원자들의 핵들 모두와 전기적 인력으로 서로 끌어당기고 있습니다. 그러므로 공유 결합으로 이루어진 물질은 물에 녹거나 가열하여 액체 상태가 될 때에도 각각의 원자는 결합된 상태, 분자 그대로 한 덩어리처럼 행동하게 되죠. 예를 들어 설탕은 공유 결합 물질로 이온 결합과 달리 전기적 인력이 작용하여 강하게 결합되어 있지 않고, 분자들 각각이 서로 연결되어 있기 때문에 소금보다 낮은 온도에서 녹습니다. 물에 녹아도 역시 공유 결합으로 이루어진 중성의 분자들 각각으로 존재하기 때문에 전기가 통하지 않죠.


이와 같이 공유 결합된 물질들의 특징을 살펴보면 전기 전도성이 없는 경우가 대부분입니다. 다만, 탄소원자로만 이루어진 동소체(한 종류의 원자로만 이루어졌으나 그 성질이 여러가지인 물질)에서 일부는 예외가 되죠. 탄소 원자는 전자가 4개인데, 흑연, 그래핀 등은 탄소 원자들이 각각 주위의 세개 탄소 원자들과 공유 결합이 되어 있습니다. 이로 인해 남게 되는 한개의 전자는 자유전자가 되어서 전기 전도도를 올려주죠. 또한 녹는점과 끓는점이 낮은 경우가 많은데, 이는 공유 결합이 원자들간의 결합을 이루고 분자들간은 약한 결합이나 혹은 결합이 잘 이루어지지 않는 경우가 다반사이기 때문이죠. 이와 함께 탄성이 강하며, 소성 변형은 거의 일어나지 않아 연성이 없습니다. 밀도는 대부분 낮은 편이죠.


고체를 이룰 경우, 분자 결정과 원자 결정, 두 종류가 나타납니다. 분자 결정의 경우, 분자들 각각이 모양을 유지하며 분자들간에는 약한 결합 등이 형성, 배열되고 있기 때문에 약한 힘에도 부서지고 녹는점과 끓는점이 낮은 경향이 있습니다. 반면에 원자 결정은 원자들이 계속 이어지면서 그물처럼 공유 결합으로 연결이 되어 거대 분자, 즉 큰 단결정을 이루고 있는 상태로 결합력이 매우 강합니다. 무수히 많은 물질, 화합물들이 공유 결합을 하고 있습니다. 우리가 가장 쉽게 접할 수 있는 물에서부터 탄화 수소와 다양한 탄소 화합물들, 특히 가장 단단한 결정인 다이아몬드, 흔히 쓰이는 반도체 소재인 실리콘(Si) 등을 들 수 있죠. 이에 더하여 여러 화합물 반도체들, ZnS, ZnSe, CdS, CdTe 등(이상, II-VI족 화합물), GaP, GaN, AlP, AlAs, InP, InAs 등(이상, III-V족 화합물), 그리고 SiGe, SiC 등(이상, IV-VI족 화합물)이 대표적입니다.
# 참고로 하고 있는 여러 자료의 도움에 감사를 표하며, 계속 업그레이드 됩니다.
# 의견과 조언, 수정과 요청은 늘 환영합니다. 댓글이나 전자메일로~ bkju@korea.ac.kr
# 저작자, 본 사이트를 반드시 표시, 비영리적으로만 사용할 수 있고, 내용 변경은 금지합니다.
풀어보기

더! 공부하기
'공부와 생각들 > 전자재료 소자' 카테고리의 다른 글
| 1-9. 약한 결합, 고체 (0) | 2020.01.07 |
|---|---|
| 1-8. 금속 결합, 고체 (0) | 2020.01.07 |
| 1-6. 이온 결합, 고체 (0) | 2020.01.07 |
| 1-5. 화학적 결합, 고체 만들기 (0) | 2020.01.07 |
| 1-4. 주기율표 (0) | 2020.01.07 |